单细胞转录组的非模式物种时代 返回
10X单细胞转录组技术自问世以来,围绕人和小鼠等模式物种的研究居多,但随着技术的不断成熟和发展,单细胞转录组技术向非模式物种研究领域拓展是必然趋势。从单细胞层面解析非模式物种不论是对发育生物学、生态学的发展还是物种起源和进化都具有重要的推动作用。目前非模式物种的单细胞研究虽数量少,但增长趋势十分明显,仅2020年下半年比上半年增加了27篇,其中不乏Cell、Science、Nature这样的顶级期刊,由此可见,单细胞转录组已逐步向非模式物种时代迈入!
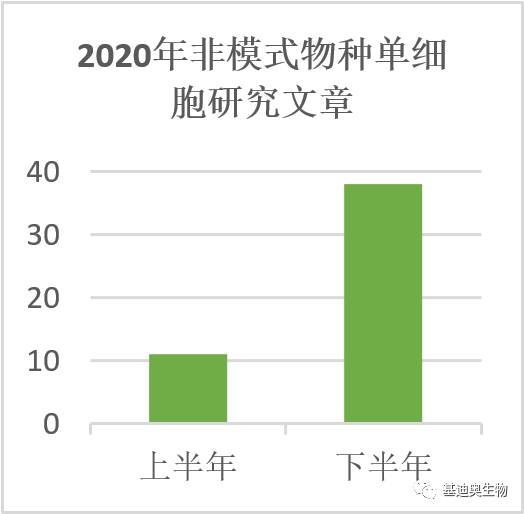
10X官网数据统计结果
非模式物种单细胞转录组研究核心优势在于“新”,这个新包含了两个方面:
1.新的领域,单细胞转录组解析非模式物种是前人未曾研究或研究较少的领域,有利于我们开展细分领域的首篇单细胞转录组文章,例如2020年11月基迪奥客户借助单细胞转录组技术首次解析了罗非鱼头肾免疫细胞图谱,打响水产经济鱼类单细胞转录组研究第一枪(往期文章:打响水产鱼类单细胞测序文章第一枪)。
2.新的技术,10X单细胞转录组技术虽然已经发展了近6年,但大多数分析内容都是围绕人和小鼠开发的,因此针对非模式物种的单细胞转录组技术尚处于发展初期,文章结构类似于早期的模式物种单细胞文章,分析内容基本以图谱绘制为主,再利用拟时分析简析谱系分化,最终分子实验加以验证,就可以发表一篇较好的文章。
今年2月由基迪奥合作客户华南农业大学聂庆华、张细权教授团队发表在Journal of Pineal Research杂志上,有关褪黑激素与鸡前体脂肪细胞分化异质性关系的文章,就是典型的非模式物种单细胞转录组文章结构。
文章首先借助单细胞转录组技术,绘制了褪黑激素作用前后鸡前体脂肪细胞图谱,通过细胞频率分析发现褪黑激素作用后cluster0细胞数明显减少,cluster1细胞数显著增加,利用拟时分析探究褪黑素作用后cluster1细胞分化命运,发现了褪黑激素促进了鸡前体脂肪细胞向脂质分解代谢分支方向分化,最终利用小鼠体内实验和分子实验验证了褪黑激素通过下调G0S2基因的表达促进脂肪分解,同时上调FABP4基因的表达抑制脂肪生成。
基迪奥生物在此项目中,为客户提供了从细胞标记、建库测序、数据挖掘到图形绘制等全程技术支持!
接下来我们一起来看一下文章的详细内容~

合作单位:华南农业大学
发表期刊:Journal of Pineal Research
影响因子:14.528
研究背景:
肥胖是一种复杂的慢性疾病,已成为一种全球健康流行病,而睡眠不足引起的褪黑激素分泌缺陷是导致肥胖的原因之一,并且有研究报道褪黑激素在预防肥胖及其并发症方面的潜力,然而,其具体的分子机制以及褪黑激素与前体脂肪细胞分化异质性的关系尚不清楚。文章旨在利用单细胞转录组技术,探究褪黑激素作用前后前体脂肪细胞分化轨迹变化,揭示褪黑激素治疗肥胖的分子作用机制。
研究方法:
文章以鸡为研究对象,将雏鸡随机分为两组,每组各3只,实验组以添加褪黑素的饮用水饲养,对照组以无褪黑素的饮用水饲养,取雏鸡腹部白色脂肪组织,0.1mg/mL胶原酶I酶解消化制备单细胞悬液,用于10X Genomics单细胞转录组建库。
研究思路:
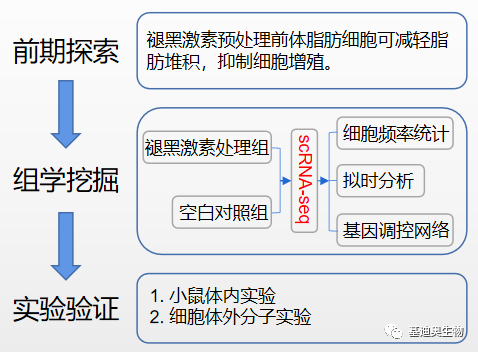
结果解读:
1.褪黑素作用前后鸡前体脂肪细胞图谱绘制
文章一共收集褪黑素处理组(Mel)和空白对照组(Con)25,071个前体脂肪细胞进行了单细胞转录组测序,细胞聚类分群得到14个亚群(图1A)。细胞频率统计结果显示,褪黑激素作用后cluster0细胞数明显减少,cluster1细胞数显著增加(图1B),因此作者推测cluster0和cluster1之间细胞频率的显著变化可能在脂肪形成和脂肪分解中发挥重要作用。
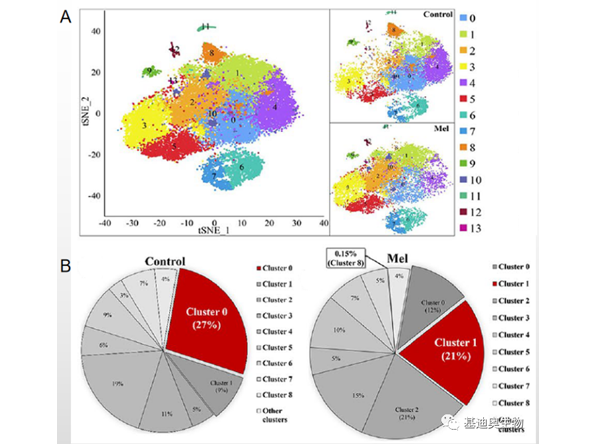
图1 鸡前体脂肪细胞全局细胞图谱
2.目标亚群基因表达特征分析
基于上述推测,作者进一步分析了cluster0和cluster1的基因表达特征,差异基因表达分析结果显示,抑制脂肪分解相关基因G0S2在cluster0中显著高表达,因此作者重新定义cluster0为G0S1﹢cluster,cluster1为G0S2﹣cluster(图2A),同时发现,抑制脂肪生成相关基因GATA2、KLF2、KLF3、KLF7和FABP4在G0S2﹣cluster中显著高表达(图2B)。综上,作者推测,褪黑激素通过调节G0S2﹣cluster(cluster1),发挥促进脂肪分解、抑制脂肪合成的作用。
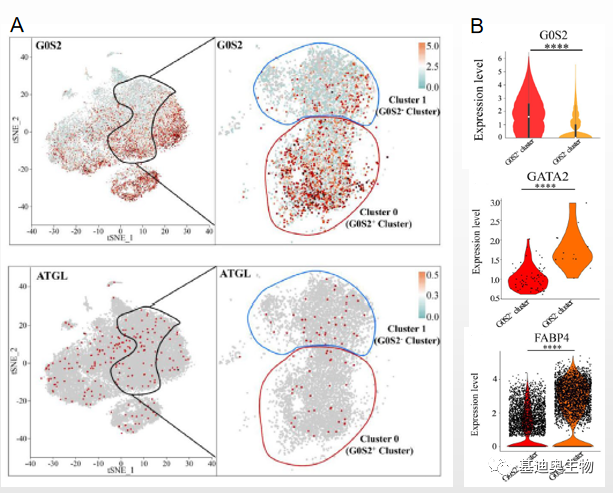
图2 G0S2﹣cluster(cluster1)基因表达特征
3.目标亚群拟时分析
紧接着,作者借助拟时分析探究褪黑激素对G0S2﹣cluster(cluster1)细胞分化命运的影响,拟时间轨迹分析结果显示,褪黑激素处理组细胞分布在Cell fate1/2两个不同的分支轨迹上,而对照组细胞主要分布在Pre-branch分支起点,无明显分化迹象(图3A);分支差异基因分析结果显示,Cell fate1分支差异基因主要富集在脂质分解代谢term(图3C),并且在Cell fate1中抑制脂肪合成相关基因FABP4的表达量随拟时间值增加而增加(图3B)。拟时分析结果表明褪黑激素可重编程前体脂肪细胞的分化轨迹,并诱导参与脂质分解代谢的Cell fate 1分支的产生。
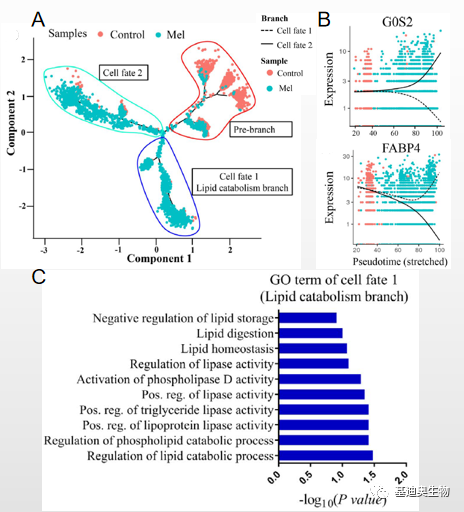
图3 拟时分析揭示褪黑激素对前体脂肪细胞分化命运的影响
4.分子实验验证
文章最后,作者在小鼠前脂肪细胞3T3-L1细胞系中,利用G0S2过表达载体以及合成G0S2﹣siRNA,分别构建了G0S2过表达和敲低细胞系,从过表达和敲低两个层面揭示G0S2在前体脂肪细胞中的功能。过表达实验结果显示,G0S2抑制了脂肪分解关键基因ATGL的表达,促进脂肪合成相关基因C/EBPα、C/EBPβ、PPARγ的表达(图4A);siRNA干扰实验结果显示,G0S2敲低促进了ATGL上调表达,C/EBPα、C/EBPβ、PPARγ下调表达(图4B)。作者最终从分子水平上验证了褪黑激素通过调节G0S2促进脂肪分解,抑制脂肪合成。
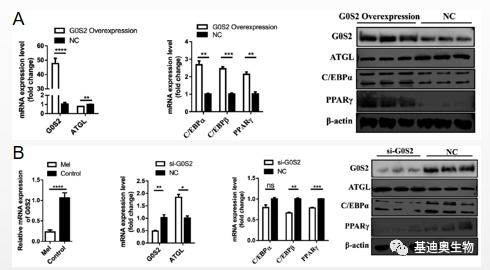
图4 qPCR/western blot验证G0S2在前体脂肪细胞中的功能
这篇文章整体研究思路清晰,机制解析透彻,是一篇值得学习参考的优秀文献!并且,作者首次从单细胞层面揭示了褪黑激素对鸡前体脂肪细胞分化的影响,为肥胖症的研究提供了一种新的思路,为非模式物种的研究提供了一个新的方向。
而基迪奥生物具备多年的单细胞项目经验,从悬液制备、序列比对到细胞注释总结了一整套的解决方案,克服了非模式物种由于研究较少,先验知识不足的困难,期待助力您轻松开展非模式物种单细胞项目!