转录组和广泛靶向代谢组揭示了纳米塑性毒性诱导美洲杨的代谢变化
|
合作单位:河北农业大学
发表期刊:Journal of Hazardous Materials
|
|
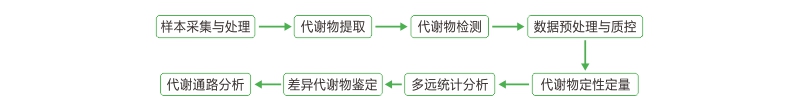
目的:全球越来越关注普遍存在的塑料污染问题。研究了杨树(Populus × euramericana cv)的响应。通过表型、微观解剖、生理、转录组学和代谢组学方法研究纳米塑性毒性。
取材:分别收集对照组、200NP组、400NP组、600NP组和800NP组的叶片进行转录组和广靶代谢组检测
结果: 1、:DEGs鉴定: 通过DESeq2软件分析,在对照组与各PS-NPs处理组之间共鉴定出3854个差异表达基因 (DEGs),其中上调基因数量远多于下调基因。GO富集分析: PS-NPs对Poplar 107的转录组产生了广泛的影响,包括转录调控活性、催化活性、代谢过程等,涉及初级和次级代谢途径。
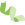
2、DAMs鉴定: 通过UPLC-MS/MS技术,在对照组与各PS-NPs处理组之间共鉴定出318个差异积累代谢物 (DAMs),其中上调DAMs数量远多于下调DAMs。 KEGG富集分析:400NP组 vs. 对照组: DAMs主要与初级代谢过程相关。800NP组 vs. 对照组: 上调DAMs主要与次级代谢(尤其是黄酮类生物合成)相关,下调DAMs主要与初级代谢相关。400NP组 vs. 800NP组: 上调DAMs主要与次级代谢相关,下调DAMs主要与有机酸及其衍生物相关。三组共有的DAMs: 上调DAMs主要与脂肪酸降解和黄酮类生物合成相关,下调DAMs主要与碳固定和氨基酸生物合成相关。
3、共同富集通路: 13个KEGG通路在转录组和代谢组数据中都有富集,其中10个通路在转录组水平上富集,1个通路(黄酮类生物合成)在代谢组水平上富集。黄酮类生物合成通路: 在800NP组中,与黄酮类生物合成相关的DEGs和DAMs表达水平显著上调,表明植物在严重PS-NPs胁迫下会激活黄酮类生物合成途径以应对氧化损伤。RT-qPCR验证: 对12个黄酮类生物合成相关DEGs进行RT-qPCR验证,结果显示这些基因在800NP组中的表达水平显著高于对照组和400NP组,进一步证实了转录组数据的可靠性。
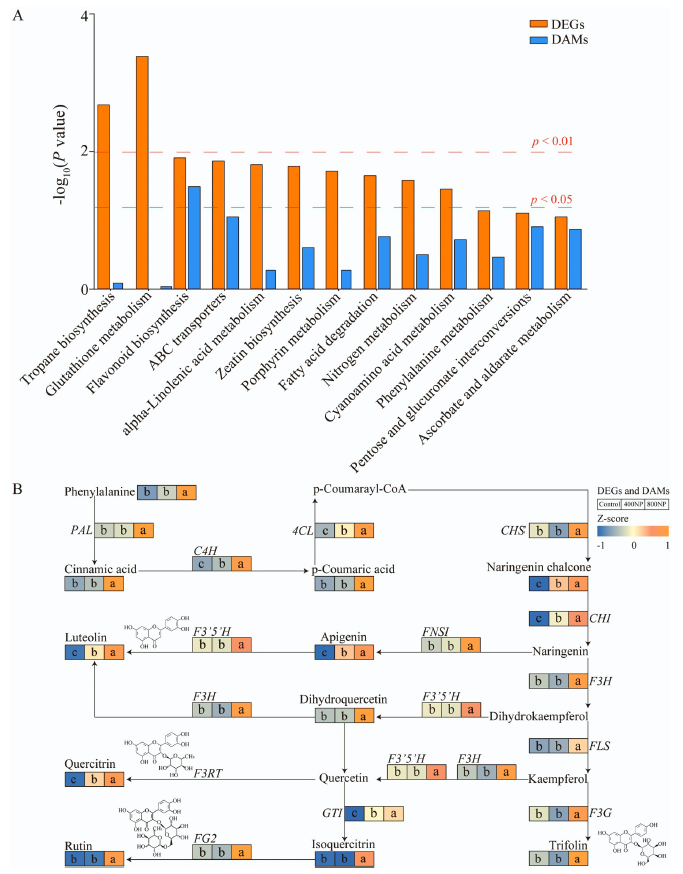
图1 PS-NP处理的美洲杨转录组与代谢组数据关联分析
|
|
参考文献
Xu, Liren, et al. "Nanoplastic toxicity induces metabolic shifts in Populus× euramericana cv.'74/76'revealed by multi-omics analysis." Journal of Hazardous Materials 470 (2024): 134148.
|